HOVEDFUNN
Ti av tretten gravide pasienter innlagt ved Rikshospitalets intensivenheter med akutt respirasjonssvikt utløst av covid-19 ble intubert etter terapisvikt med non-invasiv mekanisk ventilasjon.
Alle pasientene oppfylte kriterier for ARDS.
Alle pasientene overlevde sykehusoppholdet, men det var to tilfeller av intrauterin fosterdød.
Nær halvparten av pasientene anga moderat til sterkt redusert egenopplevd helse og livskvalitet 15 måneder etter intensivoppholdet.
Akutt, alvorlig respirasjonssvikt er en vanlig årsak til intensivmedisinsk behandling blant pasienter med covid-19. I Norge har dødeligheten blant kritisk syke vært moderat (1), men overlevende har økt risiko for senkomplikasjoner, kalt postintensivbehandlingssyndrom (post-intensive care syndrome). Dette gjelder særlig pasienter som i forløpet av sykdommen utvikler ARDS (acute respiratory distress syndrome / akutt lungesviktsyndrom) (2).
I svangerskapet utgjør akutt respirasjonssvikt som komplikasjon til covid-19 en livstruende tilstand både for mor og for foster (3). Denne rapporten beskriver karakteristika, behandling og forløp hos gravide kvinner henvist til Rikshospitalet på grunn av respirasjonssvikt utløst av covid-19.
Materiale og metode
Gravide med covid-19 ble registrert ved innleggelsen i perioden mars 2020 til mai 2023. Rikshospitalet har ikke landsfunksjon for kritisk syke gravide, men har i dialog med andre sykehus tatt imot pasienter der risikoen for mor og foster har vært vurdert som særlig stor og der vurdering av ECMO-behandling har vært aktuelt. Vi gjennomgikk pasientenes journalopplysninger i ettertid og beskriver kliniske forløp, behandlingsparametere og laboratoriedata fra intensivoppholdet.
Etter 15 måneder ble pasientene fulgt opp med spørsmål om selvopplevd helse og livskvalitet, samt symptomer på posttraumatisk stress, vurdert med skåringsverktøyene EQ-5D-5L (Euro Quality of Life – Five-Dimensions – Five Levels) og IES-6 (Impact of Event Scale-6) (4, 5). Verdier er presentert som gjennomsnitt eller medianverdi, med spredningsmål som minimums- og maksimumsverdi hvis ikke annet er oppgitt. Vi har benyttet Stata versjon 17.0 og Microsoft Excel som analyseverktøy.
Studien er godkjent av Regional komité for medisinsk og helsefaglig forskningsetikk (REK) Sør-Øst (REK nummer 630377) og personvernombudet ved Oslo universitetssykehus. Alle pasienter har gitt informert samtykke.
Resultater
13 gravide med akutt respirasjonssvikt utløst av covid-19 ble innlagt i perioden februar til desember 2021. Ingen av kvinnene var vaksinert mot SARS-CoV-2. Ti kvinner hadde innvandrerbakgrunn (6). Sykdomsvarigheten før innleggelse varierte fra ett til elleve døgn etter symptomdebut. Alle pasientene oppfylte kriterier for ARDS, med liten grad av komorbiditet (tabell 1).
Tabell 1
Pasient- og behandlingskarakteristika for 13 gravide med akutt respirasjonssvikt utløst av covid-19 og innlagt ved Oslo universitetssykehus, Rikshospitalets intensivenheter i perioden mars 2020 til mai 2023. Verdier er angitt som median (min – maks) dersom annet ikke er angitt.
| Pasient- og behandlingskarakteristika | Verdi | Referanseverdier | |
|---|---|---|---|
| Alder (år) | 33 (22–42) | - | |
| Vekt ved innleggelse (kg) | 74 (60–96) | - | |
| Høyde (cm) | 161 (150–170) | - | |
| Kroppsmasseindeks (kg/m2) | 29 (24–37) | - | |
| Paritet (antall) | 1 (0–3) | - | |
| Gestasjonsalder (uker) | 27 (24–35) | - | |
| Komorbiditet (antall) | - | ||
| Muskel- og skjelettplager | 5 | - | |
| Psykiske plager | 4 | - | |
| Endokrin sykdom | 4 | - | |
| Annet | 3 | - | |
| SAPS II-skår1 | 38 (21–70) | - | |
|
|
|
| |
| Laboratoriefunn ved innleggelse | |||
| Hemoglobin (g/dL) | 9,7 (8,1–11,9) | 11,7–15,3 | |
| Leukocytter (× 109/L) | 8,0 (6,1–18,3) | 3,5–10 | |
| Nøytrofile granulocytter (× 109/L) | 6,9 (5,1–16,5) | 1,5–7,3 | |
| Trombocytter (× 109/L) | 231 (155–312) | 145–390 | |
| D-dimer (mg/L) | 1,2 (0,5–10) | < 0,50 | |
| Fibrinogen (g/L) | 4,7 (3,1–6,3) | 1,9–4,0 | |
| Laktatdehydrogenase (U/L) | 353 (241–562) | 105–205 | |
| Ferritin (µg/L) | 126 (42–825) | 10–170 | |
| C-reaktivt protein (mg/L) | 74 (38–166) | < 4 | |
| Prokalsitonin (µg/L) | 0,2 (0,0–1,0) | < 0,10 | |
| Kreatinin (μmol/L) | 36 (26–71) | 45–90 | |
| Bilirubin (μmol/L) | 8 (4–26) | 5–25 | |
| Perifer oksygenmetning (SaO2) (%) | 96 (88–100) | 97–100 | |
| Laktat (mmol/L) | 1,0 (0,5–1,9) | 0,5–2,3 | |
|
|
|
| |
| Behandlingsdata | |||
| Liggetid i sykehus (døgn) | 16 (10–83) | - | |
| Liggetid i intensivavdeling (døgn) | 8 (4–35) | - | |
| Invasiv respiratorbehandling (døgn; n = 10) | 8 (1–25) | - | |
| Non-invasiv respirasjonsstøtte (døgn; n = 13) | 1 (0–2) | - | |
| P/F-ratio2 (kPa; n = 10) (ved innleggelse) | 14 (9–36) | > 50 | |
| Høyeste topptrykk (cm H2O; n = 10) | 29 (23–32) | - | |
| PEEP (cm H2O; n = 10) | 11 (8–15) | - | |
| Tidevolum (mL/kg forventet kroppsvekt (PBW); n = 10) | 6,1 (2,5–7,4) | - | |
1SAPS II = simplified acute physiology score, 2. utgave. Sigmoid skala 0–150 poeng, der 38 poeng (median) motsvarer forventet sykehusdødelighet på ca. 20 %, 21 poeng motsvarer sykehusdødelighet på ca. 5 %, 70 poeng motsvarer sykehusdødelighet på ca. 80 %.
2P/F-ratio = forholdstallet mellom partialtrykket av oksygen i arterieblod (PaO2), angitt i kilopascal, og fraksjonen av oksygen i innåndingsluften (FiO2). PBW, predicted body weight (45,5 + (0,91 x [høyde i centimeter – 152,4])).
Ti pasienter ble oralintubert etter terapisvikt med non-invasiv mekanisk ventilasjon. Alle de intuberte pasientene ble behandlet med volum- og trykkbegrenset ventilasjon (tabell 1). Fem pasienter ble behandlet i modifisert bukleie. Ni pasienter ble behandlet med muskelrelaksantia og alle fikk kortikosteroider.
Hos én tidligere frisk kvinne i slutten av 20-årene ble det besluttet å etablere venovenøs ECMO-behandling etter at konvensjonell lungebeskyttende respiratorbehandling med dyp sedasjon, muskelrelaksantia, bukleie og NO-gass ikke førte frem. ECMO-behandlingen kunne avvikles etter 17 døgn. Pasienten ble ekstubert etter totalt 25 døgn med invasiv ventilasjonsstøtte og ble forløst med keisersnitt fem uker før termin.
Median liggetid i Rikshospitalets intensivenheter var åtte dager (tabell 1). Samtlige pasienter hadde énorgansvikt. To pasienter fikk akutte komplikasjoner: lungeembolisme og ikke-behandlingskrevende pneumotoraks. Syv intuberte pasienter hadde koinfeksjoner som ble behandlet med antibiotika.
Svangerskapet
Ved innleggelse på Rikshospitalet var kvinnene gravide i andre eller tredje trimester (tabell 1). Vi hadde ikke holdepunkter for at mors prognose ville forbedres av forløsning. I de fleste tilfellene var vår vurdering at kontinuasjon av svangerskapet var nødvendig for å unngå alvorlig prematuritet og for å sikre fosterets lungemodning med steroider i to døgn. Alle pasientene ble overvåket med daglig kardiotokografi (CTG) og/eller ultralydundersøkelse. Det ble etablert beredskapsplaner for perimortem sectio med smittevernhensyn.
Tre kvinner ble forløst med sectio under pågående respiratorbehandling grunnet økende oksygenbehov, gjentatt desaturering og hemodynamisk instabilitet. To kvinner ble forløst vaginalt etter intrauterin fosterdød. Hos disse to viste patologisk undersøkelse av placenta subakutt placentitt og maternell vaskulær malperfusjon.
Egenrapportert helse og livskvalitet
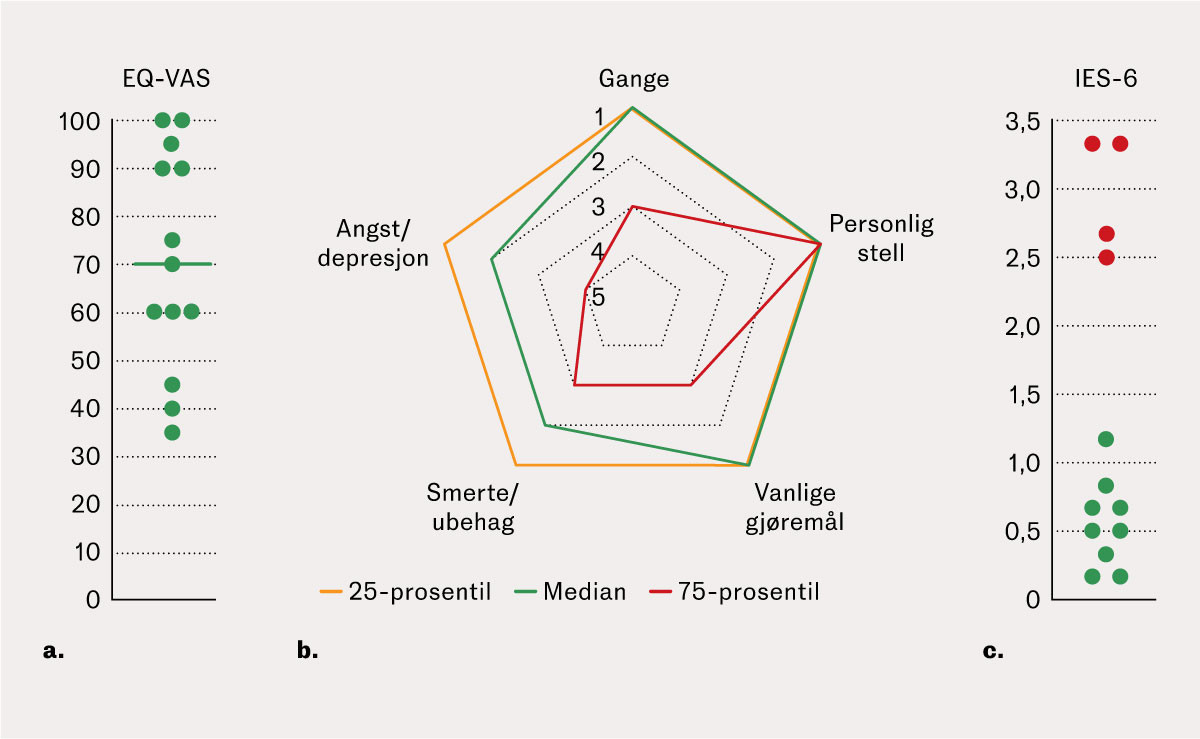
Medianverdi for egenvurdert helse (EQ-VAS) var 70 (35–100) (figur 1a). Pasientene anga minimale plager knyttet til personlig stell, mens smerter/ubehag og angst/depresjon var fremtredende (figur 1b). Symptomer på posttraumatisk stress var vanligst hos kvinner som hadde rapportert tidligere psykiske helseplager (figur 1c).
Diskusjon
Gravide kvinner med covid-19 har trolig økt risiko for utvikling av alvorlig sykdomsforløp, spesielt ved enkelte virusvarianter (deltavirus) (7). I Norge har imidlertid samtlige gravide kvinner med covid-19 innlagt i intensivavdeling overlevd intensiv- og sykehusoppholdet (n = 30, upubliserte data fra Norsk intensiv- og pandemiregister) (8). Det er et bærende prinsipp i fødselshjelpen at alvorlig sykdom hos gravide vurderes for behandling på lik linje med ikke-gravide, men det er utfordrende å veie forlengelse av svangerskapet for å unngå ekstrem prematuritet opp mot eventuell forløsning og svangerskapsavbrudd for å bedre mors behandlingsutsikter. Nyere internasjonale data støtter vår beslutning om å fortsette svangerskapet hos våre pasienter (9).
Ingen av kvinnene i vårt materiale var vaksinert mot covid-19. Vaksine til gravide var ikke anbefalt ved oppstart av vaksineprogrammet i desember 2020, og først i januar 2022 fikk alle gravide kvinner tilbud om vaksine uavhengig av svangerskapets varighet (10). Skiftende vaksineråd, lite målrettet informasjon og bekymring for bivirkninger kan ha medvirket til at gravide kvinner ikke ble vaksinert, selv etter endringer i vaksineanbefalingene. Innvandrerbakgrunn med språk- og kulturbarrierer kan også ha påvirket holdninger til vaksinasjon i vårt pasientmateriale.
Pasientene i vårt materiale hadde primært respirasjonssvikt med begrenset påvirkning av andre organer (tabell 1). De fleste opplevde terapisvikt med non-invasiv ventilasjon (NIV) og ble intubert. Mekanisk ventilasjon er en bærebjelke i behandling av ARDS og skal gjennomføres skånsomt for å unngå ytterligere lungeskade (11). Det er gitt sterk anbefaling om bruk av kortikosteroider (deksametason) ved akutt, alvorlig respirasjonssvikt utløst av covid-19 (12). Deksametason krysser imidlertid placenta, og WHO anbefaler overgang til ekvipotente doser prednisolon eller metylprednisolon etter maksimalt to dagers behandling. Slik bibeholdes også effekten av deksametason med hensyn til lungemodning hos fosteret.
ECMO-behandling av gravide er assosiert med risiko for alvorlige komplikasjoner (13) og må veies opp mot risikoen ved å fortsette konvensjonell respiratorbehandling. Vi hadde ingen tidligere erfaring med venovenøs ECMO-behandling av gravide kvinner med ARDS. Vi tok derfor kontakt med kollegaer tilknyttet University of Michigan og The Extracorporeal Life Support Organization (ELSO) for å få et større erfaringsgrunnlag. Her ble vi forsikret om at våre standardprosedyrer er gyldige også for gravide.
Langtidsoppfølging av intensivpasienter er anbefalt for å avdekke symptomer på postintensivbehandlingssyndrom (2). Ut over fysiske plager, som ofte kan tilskrives primærårsaken til intensivoppholdet, er mentale og kognitive helseplager viktige komponenter. I vår undersøkelse var pasientene i liten grad hemmet i daglige gjøremål 15 måneder etter intensivoppholdet, men nesten halvparten av pasientene anga uspesifikke smerter og ubehag, angst og depresjon, og én av tre opplevde posttraumatisk stress. Posttraumatisk stress var vanligere hos pasienter med tidligere psykiske helseplager. Median verdi for selvopplevd helse var sammenlignbar med funn i andre studier av tidligere intensivpasienter, mens andelen med symptomer på posttraumatisk stress var noe høyere (14).
Oppsummering
13 gravide kvinner ble overflyttet til Rikshospitalet med akutt, alvorlig respirasjonssvikt utløst av covid-19. Alle overlevde intensiv- og sykehusoppholdet, men hos to kvinner ble det påvist intrauterin fosterdød. Etterlevelse av gjeldende retningslinjer for skånsom respiratorbehandling har stått sentralt i vår håndtering. Litt under halvparten av pasientene rapporterte redusert livskvalitet 15 måneder etter intensivoppholdet, betinget i uspesifikke smerter og ubehag, angst og depresjon samt symptomer på posttraumatisk stress.
Artikkelen er fagfellevurdert.
- 1.
Laake JH, Buanes EA, Småstuen MC et al. Characteristics, management and survival of ICU patients with coronavirus disease-19 in Norway, March-June 2020. A prospective observational study. Acta Anaesthesiol Scand 2021; 65: 618–28. [PubMed][CrossRef]
- 2.
Herridge MS, Azoulay É. Outcomes after Critical Illness. N Engl J Med 2023; 388: 913–24. [PubMed][CrossRef]
- 3.
Lim MJ, Lakshminrusimha S, Hedriana H et al. Pregnancy and Severe ARDS with COVID-19: Epidemiology, Diagnosis, Outcomes and Treatment. Semin Fetal Neonatal Med 2023; 28: 101426. [PubMed][CrossRef]
- 4.
Herdman M, Gudex C, Lloyd A et al. Development and preliminary testing of the new five-level version of EQ-5D (EQ-5D-5L). Qual Life Res 2011; 20: 1727–36. [PubMed][CrossRef]
- 5.
Hosey MM, Leoutsakos JS, Li X et al. Screening for posttraumatic stress disorder in ARDS survivors: validation of the Impact of Event Scale-6 (IES-6). Crit Care 2019; 23: 276. [PubMed][CrossRef]
- 6.
SSB. Slik definerer SSB innvandrere. https://www.ssb.no/befolkning/innvandrere/artikler/slik-definerer-ssb-innvandrere Lest 1.12.2023.
- 7.
Favre G, Maisonneuve E, Pomar L et al. Maternal and perinatal outcomes following pre-Delta, Delta, and Omicron SARS-CoV-2 variants infection among unvaccinated pregnant women in France and Switzerland: a prospective cohort study using the COVI-PREG registry. Lancet Reg Health Eur 2023; 26: 100569. [PubMed][CrossRef]
- 8.
Helse Bergen. Norsk pandemiregister. https://www.helse-bergen.no/norsk-pandemiregister Lest 1.12.2023.
- 9.
Vasquez DN, Giannoni R, Salvatierra A et al. Ventilatory Parameters in Obstetric Patients With COVID-19 and Impact of Delivery: A Multicenter Prospective Cohort Study. Chest 2023; 163: 554–66. [PubMed][CrossRef]
- 10.
Folkehelseinstituttet. Råd og informasjon for gravide og ammende. https://www.fhi.no/ss/korona/koronavirus/coronavirus/befolkningen/rad-for-gravide-og-ammende/?term= Lest 7.12.2023.
- 11.
Claesson J, Freundlich M, Gunnarsson I et al. Scandinavian clinical practice guideline on mechanical ventilation in adults with the acute respiratory distress syndrome. Acta Anaesthesiol Scand 2015; 59: 286–97. [PubMed][CrossRef]
- 12.
WHO. Therapeutics and COVID-19: living guideline. https://www.who.int/publications/i/item/WHO-2019-nCoV-therapeutics-2022.4 Lest 7.12.2023.
- 13.
Byrne JJ, Shamshirsaz AA, Cahill AG et al. Outcomes Following Extracorporeal Membrane Oxygenation for Severe COVID-19 in Pregnancy or Post Partum. JAMA Netw Open 2023; 6: e2314678. [PubMed][CrossRef]
- 14.
Fjone KS, Buanes EA, Småstuen MC et al. Post-traumatic stress symptoms six months after ICU admission with COVID-19: Prospective observational study. J Clin Nurs 2023; 0: jocn.16665. [PubMed][CrossRef]
Aslam og kolleger deler viktige erfaringer ved behandling av alvorlig syke gravide med covid-19 i Norge i Tidsskriftet, men feilrapporterer rådene om koronavaksine til gravide i Norge.
Folkehelseinstituttet (FHI) fulgte nøye med på kunnskapen om alvorlig sykdom hos gravide fra starten av koronapandemien, og Medisinsk Fødselsregister etablerte utvidet rapportering om gravide innlagt på sykehus med covid-19. På tross av klare internasjonale anbefalinger ble gravide ekskludert fra utprøvingsstudiene for koronavaksinene (1). Land som USA og Storbritannia tilbød likevel gravide vaksine på grunn av høye smittetall og mange gravide med alvorlig sykdom, og dannet dermed kunnskapsgrunnlaget for andre lands råd (2-4).
Det var få gravide med alvorlig koronasykdom i Norge i 2020 og første halvår av 2021 i Norge (5). FHI anbefalte i januar 2021 at vaksinasjon kunne overveies for gravide med risikotilstander, og i mai også for gravide i områder med høy smittespredning. I august 2021 ble alle gravide ble anbefalt vaksine (6). På dette tidspunktet var kunnskapsgrunnlaget for sikkerheten ved vaksinasjon for mor og det ufødte barnet bedret, og andre land rapporterte samtidig om flere tilfeller av alvorlig sykdom blant gravide med deltavarianten (7). FHI hadde tett dialog og samarbeid med nasjonale fagmiljøer både før og etter at anbefalingen ble offentliggjort.
Vaksinasjonsdekningen økte raskt, og andelen fødende kvinner som hadde fått minst én vaksinedose i svangerskapet steg fra 27% i september 2021 til 70% i januar 2022 (8). Dette tyder på at norske gravide fulgte anbefalingen i stor grad. Vaksinasjonsdekningen var lavere blant enkelte innvandrergrupper, inkludert gravide blant disse. FHI jobbet målrettet med å bedre informasjonen til innvandrere generelt og gravide innvandrere spesielt. I desember 2021 ble oppfriskningsdose anbefalt til alle gravide, og gjeldende anbefaling er at alle gravide bør ta én dose av koronavaksine i 2. eller 3.trimester av svangerskapet (9).
Aslam og kolleger bekrefter at uvaksinerte gravide er utsatt for alvorlig covid-19 sykdom også i Norge, og at fortløpende overvåking av sykdomsbyrde og vaksinasjonsdekning blant gravide er viktig for å kunne målrette tiltak. FHI anbefaler både influensa- og koronavaksine til alle for å beskytte mor og barn mot alvorlig sykdom, og vil fortsette å arbeide for å nå ut med et likeverdig vaksinasjonstilbud til alle gravide.
Litteratur:
1. Heath PT, Doare KL, Khalil A. Inclusion of pregnant women in COVID-19 vaccine development. Lancet Infect Dis 2020; 9: 1007-8. doi: 10.1016/S1473-3099(20)30638-1.
2. Shimabukuro TT, Kim SY, Myers TR et al. Preliminary Findings of mRNA Covid-19 Vaccine Safety in Pregnant Persons. N Engl J Med 2021; 384: 2273-82. DOI: 10.1056/NEJMoa2104983
3. Riley LE. mRNA Covid-19 Vaccines in Pregnant Women. N Engl J Med 2021; 384: 2342-3. doi: 10.1056/NEJMe2107070
4. GOV.UK. Joint Committee on Vaccination and Immunisation: advice on priority groups for COVID-19 vaccination, 30 December 2020. https://www.gov.uk/government/publications/priority-groups-for-coronavirus-covid-19-vaccination-advice-from-the-jcvi-30-december-2020/joint-committee-on-vaccination-and-immunisation-advice-on-priority-groups-for-covid-19-vaccination-30-december-2020 Lest: 7.3.2024
5. Varpula R, Äyräs O, Aabakke AJM et al. Early suppression policies protected pregnant women from COVID-19 in 2020: A population-based surveillance from the Nordic countries. Acta Obstet Gynecol Scand. DOI: 10.1111/aogs.14808
6. FHI. Covid-19 vaksinasjonsprogrammet, Vaksinasjon av gravide. https://www.fhi.no/contentassets/3596efb4a1064c9f9c7c9e3f68ec481f/2021-08-18-vaksinasjon-av-gravide.pdf Lest 7.3.2024
7. Vousden N, Ramakrishnan R, Bunch K et al. Severity of maternal infection and perinatal outcomes during periods of SARS-CoV-2 wildtype, alpha, and delta variant dominance in the UK: prospective cohort study. BMJ Medicine 2022; 1. doi: 10.1136/bmjmed-2021-000053
8. Örtqvist AK, Dahlqwist E, Magnus MC et al. COVID-19 vaccination in pregnant women in Sweden and Norway. Vaccine 2022; 40: 4686-92. doi: 10.1016/j.vaccine.2022.06.083.
9. FHI. Covid-19 vaksinasjonsprogrammet, Delsvar på Oppdrag 49 – Vurdering av oppfriskningsdose til aldersgruppen 18-44 år. https://www.fhi.no/contentassets/3596efb4a1064c9f9c7c9e3f68ec481f/delsvar-pa-oppdrag-49---vurdering-av-oppfriskningsdose-til-aldersgruppen-18-44-ar.pdf Lest: 7.3.2024
I vår artikkel om gravide med kritisk sykdom utløst av Covid-19 (1) har vi påpekt at ingen av våre pasienter var vaksinert og vi har diskutert mulige forklaringer. Om Folkehelseinstituttets (FHI) vaksineråd skriver vi følgende: «Vaksine til gravide var ikke anbefalt ved oppstart av vaksineprogrammet i desember 2020, og først i januar 2022 fikk alle gravide kvinner tilbud om vaksine uavhengig av svangerskapets varighet.»
Vi har hentet våre opplysninger fra FHIs nettside «Råd og informasjon for gravide og ammende» (2). Denne inneholder aktuelle vaksineråd, og nederst på nettsiden finnes en «endringshistorikk» hvor følgende er angitt: «29.04.2021: Oppdatert tekst ut fra ny kunnskap. Endret råd om vaksinering av gravide til at det kan overveies hvis fordelene overgår ulempene, også for gravide i områder med høy smittespredning og som ikke har andre underliggende sykdommer.» «31.01.2022: Endret anbefaling til å gjelde alle gravide uavhengig av trimester.»
Greve-Isdahl og medforfattere hevder i sin kommentar at «I august 2021 ble alle gravide ble anbefalt vaksine.» Men i dokumentet fra august 2021, som det vises til, står det følgende: «Alle gravide bør tilbys vaksine mot Covid-19. [..] Vaksine anbefales i 2. og 3. trimester med mindre det er risikofaktorer hos mor eller stor smitterisiko som tilsier vaksinasjon i 1. trimester.» (3) Her er det altså lagt inn et forbehold om vaksinetidspunkt som noen vil oppfatte som begrensende, og så kan man diskutere hvordan ord som tilbys og anbefales oppfattes i befolkningsgrupper med svake språkkunnskaper.
Våre kollegaer på FHI bekrefter at så mange som 30% av alle gravide fortsatt ikke var vaksinert i januar 2022, altså over ett år etter starten på vaksineprogrammet. Vi synes kanskje det bør påkalle FHIs interesse i større grad enn våre formuleringer.
Litteratur:
1. Aslam TN, Barratt-Due A, Fiane AE et al. Gravide med akutt, alvorlig respirasjonssvikt utløst av covid-19. Tidsskr Nor Legeforen 2024; 144. doi: 10.4045/tidsskr.23.0615
2. Folkehelseinstituttet. Råd og informasjon for gravide og ammende. https://www.fhi.no/ss/korona/koronavirus/coronavirus/befolkningen/rad-for-gravide-og-ammende/?term= Lest 11.3.2024.
3. Folkehelseinstituttet. Covid-19 vaksinasjonsprogrammet. Vaksinasjon av gravide. https://www.fhi.no/contentassets/3596efb4a1064c9f9c7c9e3f68ec481f/2021-08-18-vaksinasjon-av-gravide.pdf Lest 11.3.2024.